医療機器新規参入の手引き
〜 製品開発の勘所を押さえる 〜
このコースは【 日経ものづくり 】主催で開催されます。
http://techon.nikkeibp.co.jp/article/SEMINAR/20150205/402675/?rt=nocnt
終了しました。
次回は来年4月です!

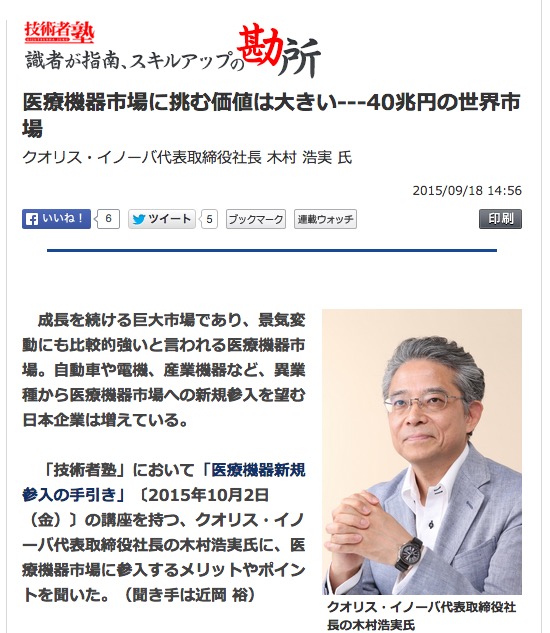
日経BP社インタビュー記事です
http://techon.nikkeibp.co.jp/atcl/column/15/417263/091800016/?ST=skillup
☆ 開催概要 ☆
日 時: 2015年10月2日(金曜) 13:30 〜 17:30
会 場: Learning Square 新橋 6F( 東京・新橋 )
主 催: 日経ものづくり
お申込: 主催者HPより直接お申し込み下さい
http://techon.nikkeibp.co.jp/article/SEMINAR/20150205/402675/?rt=nocnt
セミナー内容:
1.製品企画
医療機器のマーケティングとは
設計バリデーションの基本、カスタマーニーズと意図した用途を理解する
製品のライフサイクルマイルストーンを確立する
日本企業が知らない海外医療器機器メーカーの買収リスク
2.製品開発プロセス
医療機器はグローバル対応の設計フレームワークが必須
医療機器開発の基本、ウオーターフォールモデル
理解されていない重要な要素、設計検証と設計バリデーションの相違
要求仕様から勢品詞要所までの一貫性を示すトレーサビリティーマトリックスとは
全ての活動を根拠に基づくエビデンスで保証することの重要性
3.品質、製品不具合
トヨタ自動車のリコール問題から学ぶトップマネジメントの関わり方
テルモの出荷停止・罰金問題から学ぶマネジメントチームの関わり方
米国食品医薬品局(FDA)の警告書から判る会社の欠陥
患者や企業を守る為のインテグリティーとコンプライアンス文化
4.規制、国際標準
品質や規制に無関心なマネジメント層のマインドを変える
全社員への法規制教育は医療機器会社の生命線
専任規制・規格担当者の必要性
FDA QSRとISOの相違とは、ただ差分を理解することではない
5.プロジェクト推進
トップマネジメントが果たす大きな役割(リーダーシップ)
会社の現状を把握し、会社を変革しないとグローバル進出できない
PM(プロダクトマネジャー)とPL(プロダクトリーダー)がコンカレント開発を実現する









